Définition de loi périodique
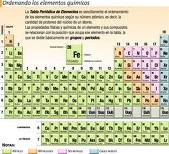
La loi périodique est la base du tableau périodique des éléments. Cette loi établie que les propriétés physiques et chimiques des éléments tendent à se répéter systématiquement au fur et à mesure que le numéro atomique augmente. Le tableau est donc un schéma qui présente les éléments chimiques suivant un ordre croissant du numéro atomique.
Le chimiste britannique John Alexander Reina Newlands (1838-1898) fut l’un des précurseurs de ce concept en émettant l’hypothèse de la loi des octaves selon laquelle dans chacun des huit éléments se retrouvent des propriétés similaires. Sous cette même idée, Newlands a publié une forme plus élaborée du tableau périodique en 1863.
Le chimiste allemand Julius Lothar Meyer (1830-1895) s’est basé sur ces notions pour déterminer les masses atomiques des éléments. Après avoir calculé les poids (masses) atomiques et mis en graphique lesdites valeurs, il a pu prouver que l’augmentation du poids atomique correspond à un accroissement des propriétés physiques. Les travaux de Meyer concernant la loi périodique ont été publiés en 1870.
Par contre, le chimiste russe Dmitri Mendeleiev (1834-1907) est celui à qui l’on doit l’honneur de la création du tableau périodique des éléments. Mendeleiev a ordonné les éléments suivant la masse atomique tout en situant dans la même colonne ceux qui avaient quelque chose en commun. Son tableau, présenté en 1869, est basé sur la variation manuelle des propriétés chimiques.
Les colonnes verticales du tableau périodique portent le nom de groupes et comprennent des éléments ayant la même valence atomique (et, de ce fait, des propriétés similaires entre eux). En ce qui leur concerne, les lignes horizontales sont les périodes et présentent des éléments ayant des propriétés différentes bien que des masses similaires.




